

软骨是没有血管的,而且软骨的再生能力很差,因此,软骨细胞和营养物质很难到达缺陷的软骨组织。逐渐磨损的关节软骨导致软骨组织的丢失,最终导致退行性关节疾病,如骨关节炎(OA)[1]。研究显示,OA是2010年第三大最常见的肌肉骨骼疾病,其中,83%的病例膝关节受累[2]。在美国,65岁及以上的成年人中,33.6%(1240万)的人患有OA。随着全球人口规模及预期寿命的延长,退行性关节疾病的发生预计也将增加[1]。因此,找到能够成功促使软骨再生的有效方法就成为一种迫切需求。
利用各种类型的干细胞进行组织再生的研究非常热门,科学家们也已经尝试着用各种来源的细胞来再生软骨,比如成体干细胞(尤其是人类间充质干细胞(hMSCs))和关节软骨细胞(ACs),但是,它们的增殖和分化潜能有限,因此限制了应用。为了克服这一局限性,科学家们正在研究用多能干细胞来再生软骨。下面就跟大家科普一下,从人类脐带血(hUCB)细胞和人类诱导的多能干细胞(hiPSCs)中获得再生软骨的能力,以及它们的优势。
UCB的优势
第一,脐带血来源丰富、容易获取。第二,收集来的脐带血污染的几率更低。第三,脐带血细胞免疫源性更低。第四,对所有脐带血均进行HLA分型检测,应用方便。第五,脐带血来源间充质干细胞(hUCB-MSCs)的倍增速度明显快于骨髓和脂肪干细胞。
hUcB-MSCs的抗炎和免疫调节作用
MSCs可以分化为骨和软骨,而且具有抗炎和免疫调节的作用。
在2010年,科学家Liu和他的团队就利用hUCB-MSCs来治疗患有类风湿关节炎的小鼠模型[8]。成纤维细胞样滑膜细胞和基质金属蛋白酶(MMPs)在炎症和软骨破坏中起着重要作用,研究证明hUCB-MSCs可以抑制滑膜细胞的增殖,而且显著降低了MMPs的含量。在小鼠体内注射hUcB-MSCs时,关节炎症状减轻,TNFa和IL-6水平也下调。
在2012年,科学家Greish证实了hUCB-MSCs在类风湿关节炎大鼠模型中的免疫调节作用[9]。注射后34天,关节炎症状减少,注射了hUCB-MSCs的组炎症细胞因子(TNFa、IFN-γ和IL-1)水平显著降低,IL-10水平升高。
CB细胞的软骨分化能力
脐带血细胞可以分化为多种细胞类型,由此被提出可以用于疾病的治疗,目前已经有研究报告了hUCB-MSCs的软骨分化能力,而且比骨髓干细胞的软骨分化能力更强。
早在2013年,科学家Jeong就证明了hUCB-MSCs是通过旁分泌的作用,促进软骨祖细胞的分化[6]。将取自OA患者的滑膜液和hUCB-MSCs联合应用,对软骨细胞的旁分泌效应增加,血小板反应素-2(TSP-2)升高,但是采用取自骨折患者的滑膜液却没有变化。而且,在应用了缺乏TSP-2的hUCB-MSCs后,小鼠的软骨组织没有得到修复。
CB细胞的软骨再生能力
脐带血采集的无伤害性以及脐带血干细胞的低免疫原性,使得hUCB-MSCs被用来进行了很多科学研究和临床试验。而且关于hUCB-MSCs促进软骨再生的研究也非常多。
在2014年,科学家Chung及其团队直接将富含hUCB-MSCs的四种水凝胶(分别是:透明质酸,海藻酸钠,聚醚,不同类型的混合物)移植到了股骨滑车槽中的软骨缺损部位[4],缺损的软骨组织都有所修复,使用透明质酸的hUCB-MSCs在大鼠关节软骨缺损中的修复率最高。同时,还单独注射了不含hUCB-MSCs的水凝胶进行了阴性对照,结果显示,应用了hUCB-MSCs的治疗组要明显优于阴性对照组。可以采用免疫染色的方法,来证实再生软骨中II型胶原的表达。在应用了hUCB-MSCs的治疗组中,再生软骨具有较高的II型胶原含量,而单独应用水凝胶的对照组却没有这种表达。
在2016年,科学家Park又将不同浓度的富含hUCB-MSCs的透明质酸水凝胶应用到了软骨组织缺损的兔子模型当中(分别是0.1/0.5/1.0/1.5 X107cells/ml)[5],植入的hUSB-MSCs在关节软骨产生的缺损内均表现出了再生特性。有趣的是,与低细胞浓度相比,细胞浓度高对软骨修复不利。细胞剂量为0.1、0.5和1.0X107cells/ml比高剂量(1.5x107cslls/ml)更有效。据此,科学家提出了两套理论:第一,过高的细胞浓度聚集,可能会造成细胞活性的降低,第二,异种免疫排斥可能会造成细胞损伤或死亡,从而影响软骨修复。
科学家Park及其团队在另一组小猪模型中也证实了hUCB-MSCs的软骨再生潜力[10]。这项研究被作为人类临床试验道路上的一个里程碑,表明了hUCB-MSCs在关节软骨缺损中具有再生能力。
后来,韩国科学家进行了一项临床试验研究,证实了使用异基因hUCB-MSCs在OA患者中进行关节软骨再生的安全性和有效性[11]。这是首次利用hUCB-MSCs在人体进行试验。7名OA患者接受了hUCB-MSCs和水凝胶的移植,在7年内均没有发生严重不良反应。其中两名患者在移植后1年内通过活检进一步检查恢复的病变,发现有白色透明状软骨的再生。
CB细胞衍生的诱导多能干细胞(iPSCs)对软骨的再生
iPSCs技术能够使分化成熟的体细胞诱导生成干细胞,这一技术影响了各个研究领域,可用于筛选药物,模拟疾病,并在临床研究中开发再生药物。(图一)
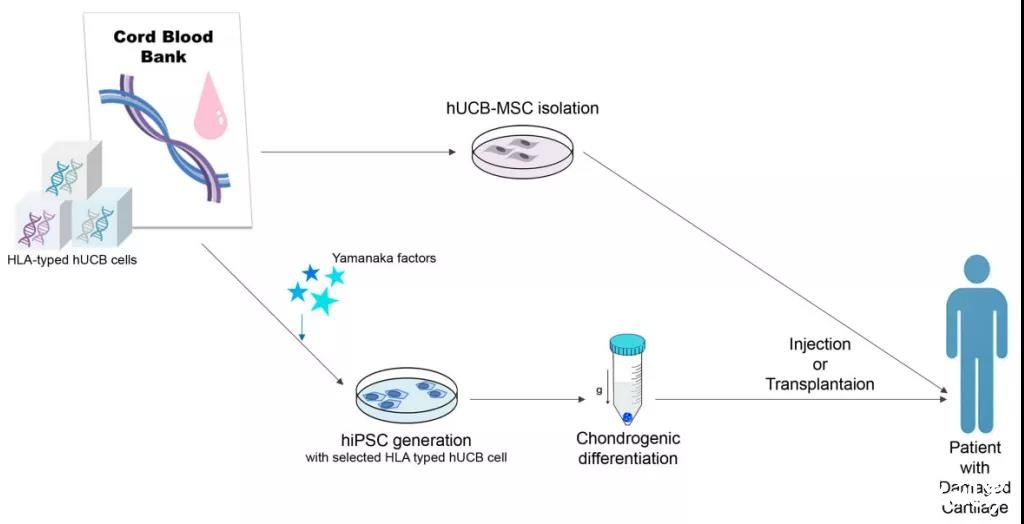
图一:使用hUCBS和hUCB-hiPSCs进行软骨发生和软骨再生的作用
在2014年,科学家Guzzo和他的团队证明了用微培养可以诱导CB细胞衍生的hiPSCs软骨形成[12]。在2017年,科学家Nam和他的团队使用hCBMC衍生的hiPSCs生成了软骨形成颗粒[13],在这项研究中,软骨特异性基因的表达随着分化从第10天到第30天的进行而增加,此外,还检测到软骨特异性标记物,如SOX9、ACAN和COL2A1。在另一项试验中,Rim证明了hCBMC-hiPSCs在大鼠骨软骨缺损模型中的修复潜力[14],分离的软骨细胞样细胞显示出类似水平的ACAN和COL2A1表达。
结语
软骨的再生能力较差,针对这一问题已经研究了几十年,在此背景下,脐带血衍生的诱导多能干细胞在未来治疗关节疾病和关节损伤方面具有巨大的潜力。

